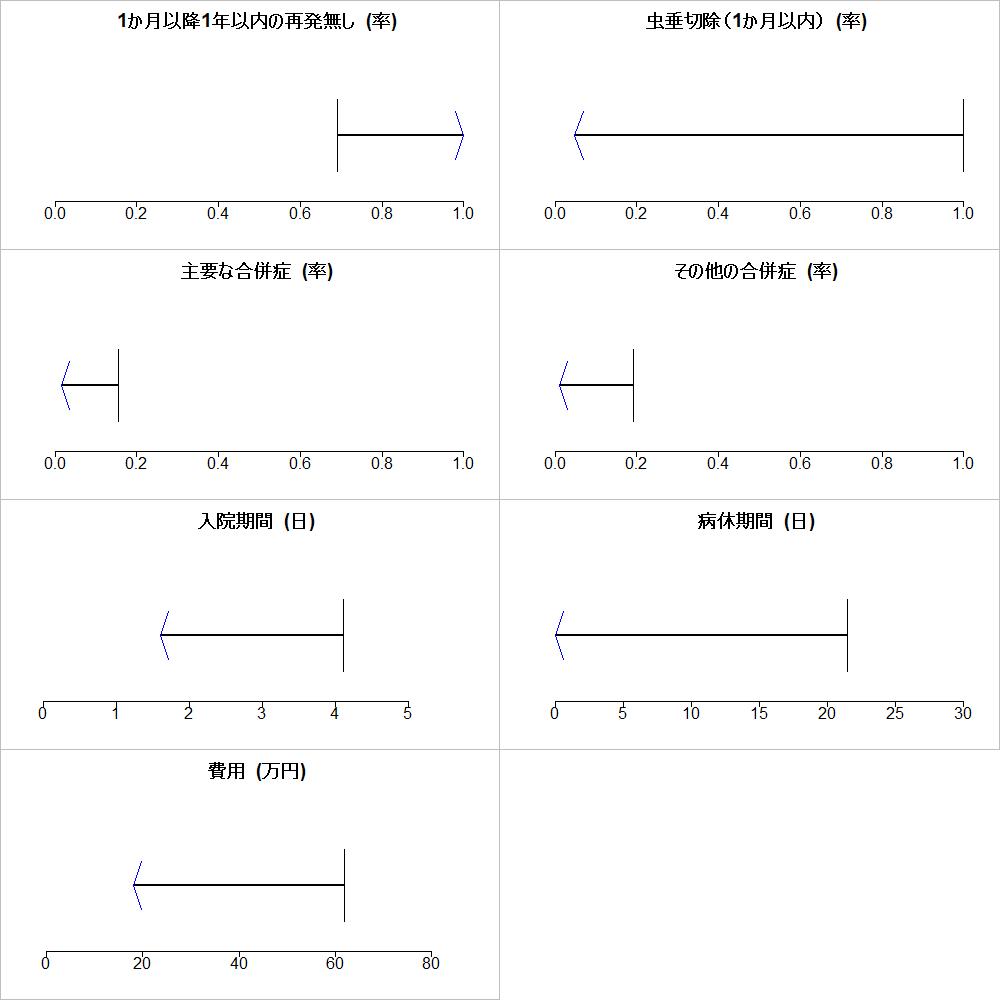
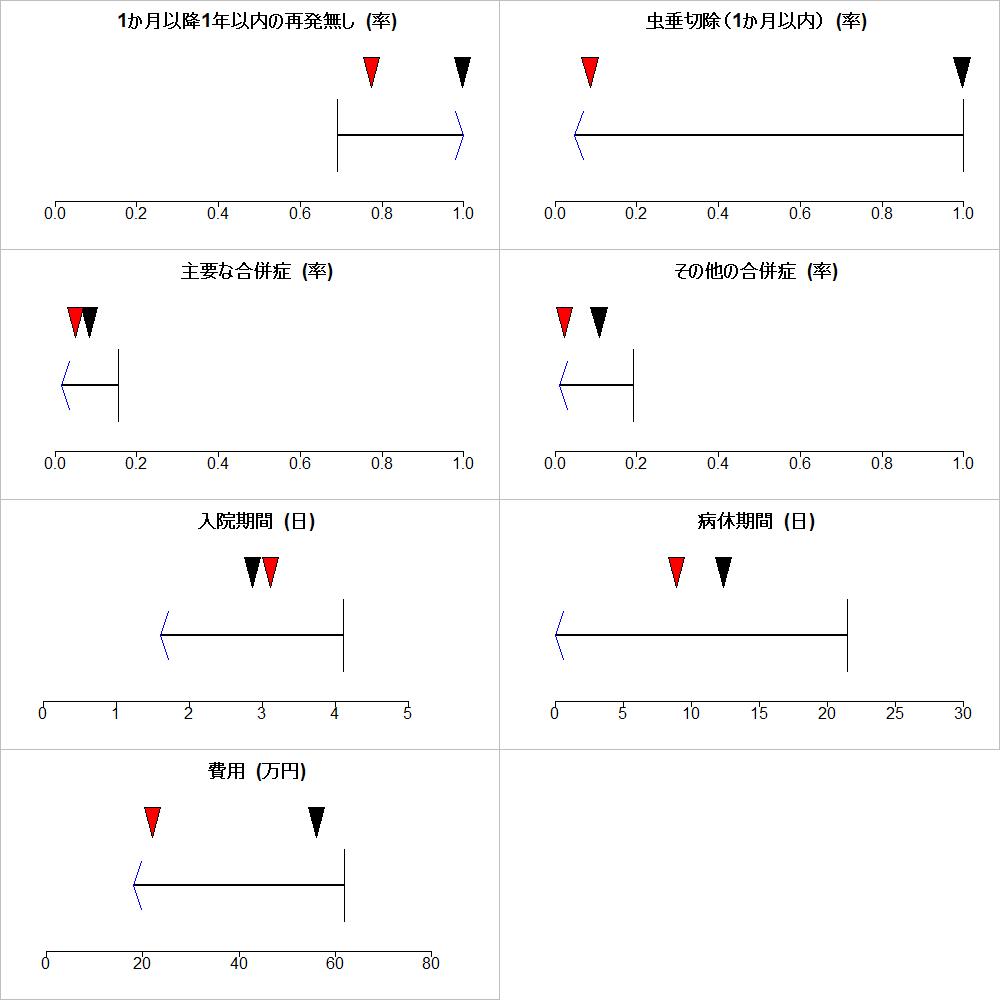
PubMedでは医学主題見出しMedical Subject Headings MeSHと呼ばれる語句が各文献にインデクサーによってインデクスされています。検索語句に対応するMeSHが同義語辞典シソーラスに含まれていれば、検索語句がその文献のタイトルやアブストラクトに含まれていなくても、そのMeSHでインデクスされている文献を探し出し、引き出すことで、同じ意味あるいは概念の語句が含まれている文献として引き出すことが可能になる仕組みです。その検索語句がMeSHであることを指示するには、語句に続けてあるいはスペースを入れて、[mh]と書きます。[mesh], [MeSH Terms]でも同じです。
MeSHはデータべース化されており、どのような用語があるか検索して調べることができます。また、MeSHは概念の広さによって、階層化されています。Decision Makingに関連する用語がMeSHではどのように扱われているか調べてみました。
MeSH用語、定義と導入された年度、Entry Terms、その他について紹介します。Entry Termsは一部のみ示します。取り上げた語句は、Decision Making, Clinical Decision-Making, Decision Support Techniques, Cost-Benefit Analysis, Patient Preference, Risk Assessment, Outcome Assessment (Health Care), Patient Outcome Assessment, Patient Harm, Safetyです。
なお、Entry Termというのはその語句をMeSHとして指定してPubMedを検索するとそれに対応したMeSH Termに置き換えられて検索が行われるものです。例えば、medical decision making[mh]で検索すると、対応するMeSH TermはClinical Decision-Makingなので、”clinical decision-making”[MeSH Terms]で実際の検索が行われます。
Decision Making
The process of making a selective intellectual judgment when presented with several complex alternatives consisting of several variables, and usually defining a course of action or an idea.
Shared Decision Making
Shared Decision Makings
*shared decision making AND 2019[dp]で検索すると実際の検索式はAutomatic Term Mapping (ATM)が作動して、(“decision making”[MeSH Terms] OR (“decision”[All Fields] AND “making”[All Fields]) OR “decision making”[All Fields] OR (“shared”[All Fields] AND “decision”[All Fields] AND “making”[All Fields]) OR “shared decision making”[All Fields]) AND 2019[dp]で行われ3648件ヒットします。shared decision making[mh] AND 2019[dp]とMeSH Termであることを指定すると、”decision making”[MeSH Terms] AND 2019[dp]で検索が実行され171件のみになります。
Clinical Decision-Making
Process of formulating a diagnosis based on medical history and physical or mental examinations, and/or choosing an appropriate intervention.
Year introduced: 2016
Medical Decision Making
Clinical Decision Making
*以前のMeSHはDecision Making (1972-2015)
Decision Support Techniques
Mathematical or statistical procedures used as aids in making a decision. They are frequently used in medical decision-making.
Year introduced: 1991
Decision Aids
Decision Analysis
Decision Modeling
Clinical Prediction Rule
Decision Support Model
*Health Care Categoryの下4番目の階層でInformation Science Categoryの下5番目の階層。
Cost-Benefit Analysis
A method of comparing the cost of a program with its expected benefits in dollars (or other currency). The benefit-to-cost ratio is a measure of total return expected per unit of money spent. This analysis generally excludes consideration of factors that are not measured ultimately in economic terms. Cost effectiveness compares alternative ways to achieve a specific set of results.
Year introduced: 1976
Cost EffectivenessCost Effectiveness Analysis
*Health Care Categoryの下4番目の階層。
Patient Preference
Individual’s expression of desirability or value of one course of action, outcome, or selection in contrast to others.
Year introduced: 2010 Patient ValueはMeSHにない。
Patient Preferences
*Health Care Categoryの下5または6番目の階層。その他、Psychiatry and Psychology Categoryの下にも位置付けられている。
Risk Assessment
The qualitative or quantitative estimation of the likelihood of adverse effects that may result from exposure to specified health hazards or from the absence of beneficial influences. (Last, Dictionary of Epidemiology, 1988)
Year introduced: 1995
Benefit-Risk Assessment
Benefit Risk Assessment
Risk-Benefit Assessment
Risk Benefit Assessment
Outcome Assessment (Health Care)
Research aimed at assessing the quality and effectiveness of health care as measured by the attainment of a specified end result or outcome. Measures include parameters such as improved health, lowered morbidity or mortality, and improvement of abnormal states (such as elevated blood pressure).
Year introduced: 1992
Outcome MeasuresOutcome Measure
Outcomes Research
*GRADE ApproachはOutcome Assessment (Health Care)->Patient Outcome Assessment->GRADE Approachとして位置付けられている。
Patient Outcome Assessment
Patient-generated evaluation data of treatment outcome or interaction in healthcare environment.
Year introduced: 2014
Patient-Centered Outcomes Research
Patient Outcomes Assessment
Patient Harm
A measure of PATIENT SAFETY considering errors or mistakes which result in harm to the patient. They include errors in the administration of drugs and other medications (MEDICATION ERRORS), errors in the performance of procedures or the use of other types of therapy, in the use of equipment, and in the interpretation of laboratory findings and preventable accidents involving patients.
Year introduced: 2014
*ひとつ上の階層がSafety。
Safety
Freedom from exposure to danger and protection from the occurrence or risk of injury or loss. It suggests optimal precautions in the workplace, on the street, in the home, etc., and includes personal safety as well as the safety of property.
Year introduced: 1991(1975)
Safeties
*Safetyの一つ下の階層にSafety ManagementやPatient Harmがある。