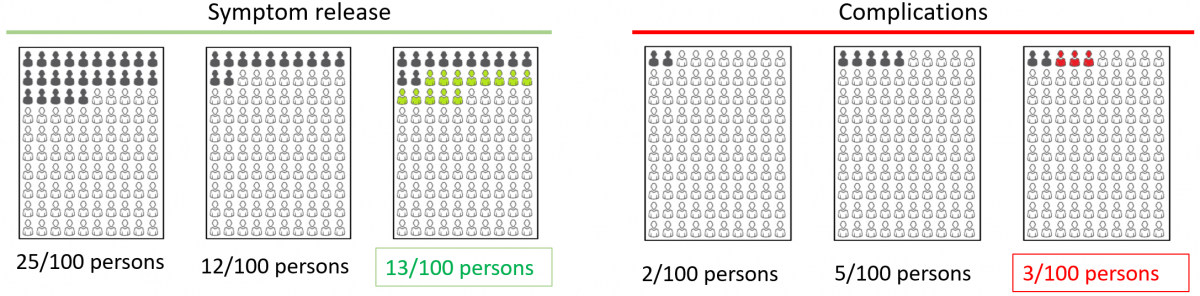
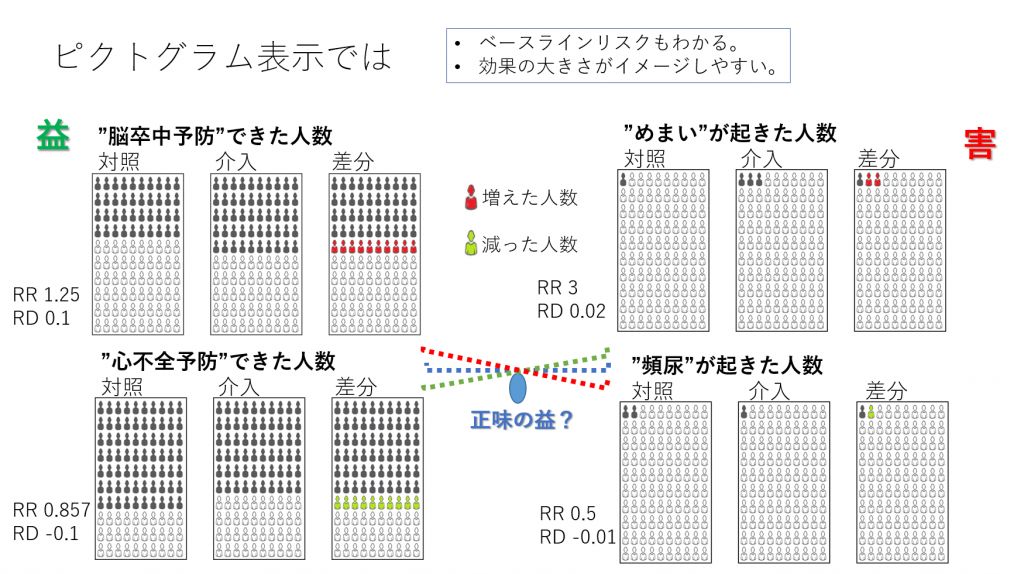
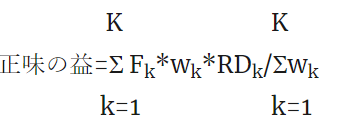Entrustable professional activities (EPA)とは”委託可能な専門的活動”のことです。研修生がその活動を監督なしで実行するために必要な能力を発揮した後に、研修生に全面的に委託することが可能な専門的実践の単位である”とされています。
アメリカ医科大学協会 Association of American Medical Colleges (AAMC)はレジデンシーに入る前に、すなわち医学部を卒業する際に、必要な13のコアEPAを提示しています。
Obeso V, Brown D, Aiyer M, Barron B, Bull J, Carter T, Emery M, Gillespie C, Hormann M, Hyderi A, Lupi C, Schwartz M, Uthman M, Vasilevskis EE, Yingling S, Phillipi C, eds.; for Core EPAs for Entering Residency Pilot Program. Toolkits for the 13 Core Entrustable Professional Activities for Entering Residency. Washington, DC: Association of American Medical Colleges; 2017. aamc.org/initiatives/coreepas/publicationsandpresentations
AAMCがどのような組織なのかは、Who We Are -AAMCに説明があります。
EPAは後述するように、複数のコンピテンスのドメインから構成されています。以前から医学部卒業生に必要なコンピテンシーが6つ挙げられていましたが、2つ追加されて8つになっています。以下の通りです。
Physician Competencies Reference Set (PCRS) – FINAL, July 2013には医師に必要なコンピテンシーのドメインとして以下の8つの項目を上げています。これらについては、上記のリンク中のCore Entrustable Professional Activities for Entering Residency: Curriculum Developers’ GuideのAppendix Cに記述されています。
1. 患者のケア(PC Patient Care): 健康問題の治療と健康増進のために、思いやりのある適切かつ効果的な、患者中心のケアを提供する。
2. 実践のための知識(KP Knowledge for Practice): 確立された生物医学、臨床医学、疫学、社会行動学に関する知識と、これらの知識を患者ケアに応用できることを示す。
3. 実践に基づく学習と改善(PBLI Practice-Based Learning and Improvement): 自己の患者ケアについて調査・評価し、科学的根拠を評価・吸収し、常に自己評価と生涯学習に基づき患者ケアを継続的に改善する能力を示す。
4. 対人関係およびコミュニケーション能力(ICS Interpersonal and Communication Skills): 患者、家族、医療従事者との効果的な情報交換や協力関係を築くための対人関係やコミュニケーション能力を発揮することができる。
5. プロフェッショナリズム(P Professionalism): 専門家としての責任を果たし、倫理的原則を遵守することを実証する。
6. システムに基づいた実践(SBP Systems-Based Practice):最適なヘルスケアを提供するために、ヘルスケアの大きな文脈とシステムに対する認識と対応、およびシステム内の他のリソースを効果的に活用する能力を実証する。
7. 専門家間のコラボレーション(IPC Interprofessional Collaboration):安全で効果的な患者・住民中心のケアを最適化するために、専門職間チーム に参加する能力を証明する。
8. 個人的および専門的な開発(PPD Personal and Professional Development:): 生涯にわたって自己および専門的な成長を維持するために必要な資質を示す。
略語:PC, KP, PBLI, ICS, P, SBP, and IPC, PPD
概念的な枠組みを構築するために、起草委員会のメンバーはまず、次のような共通認識を持ったと述べられています。
1. コンピテンシー:知識、技能、価値観、態度などの複数の要素を統合した、医療専門家の観察可能な能力。コンピテンシーは観察可能であるため、その習得を確実にするために測定・評価することができる。
2. 委託可能な専門的活動(EPA): EPAとは、専門職としての実践の単位であり、十分なコンピテンシーを獲得した研修生が、監督されずに行うことを任される業務や責任と定義される。EPAは、その過程と結果が独立して実行可能、観察可能、測定可能であり、したがって委託の判断に適している。
3. マイルストーン:マイルストーンとは、あるコンピテンシーの達成レベルを示す行動記述子である(ACGME Milestones projectによる)。
コンピテンシーとEPA(Entrustable Professional Activities)という、文献上有力な2つの概念的枠組みの利点と欠点を検討した後、起草委員会はEPAを採用することにした。なお、EPAとコンピテンシーは相互に排他的なものではないことに留意されたい。それどころか、EPA は定義上コンピテンシーの統合を必要とし、コンピテンシーは(EPA の枠組で提供できるように)パフォーマンスという文脈で評価されるのが最良である。
EPAは仕事の単位であり、コンピテンシーは個人の能力である。EPA の特徴の 1 つは、通常、領域横断的にコンピテンシーの統合を必要とすることである。この概念を本業務に適用するため、起草委員会は、13 の EPA のそれぞれについて、委託を決定するために最も重要な 5~8 のコンピテンシーを決定するためのマッピング作業を実施した。コンピテンシーは、”Reference List for General Physician Competencies “(上記の8つ)から選択した。
図1に学生から専門医までのEPAの関係を、図2にEPA, DOC, Competency, Milestoneの関係を示します。これらは、上記のリンク中のCurriculum Developers’ GuideのFigure 1, 2を翻訳したものです。Fuculty and Learners’ Guideにも同じ図があります。
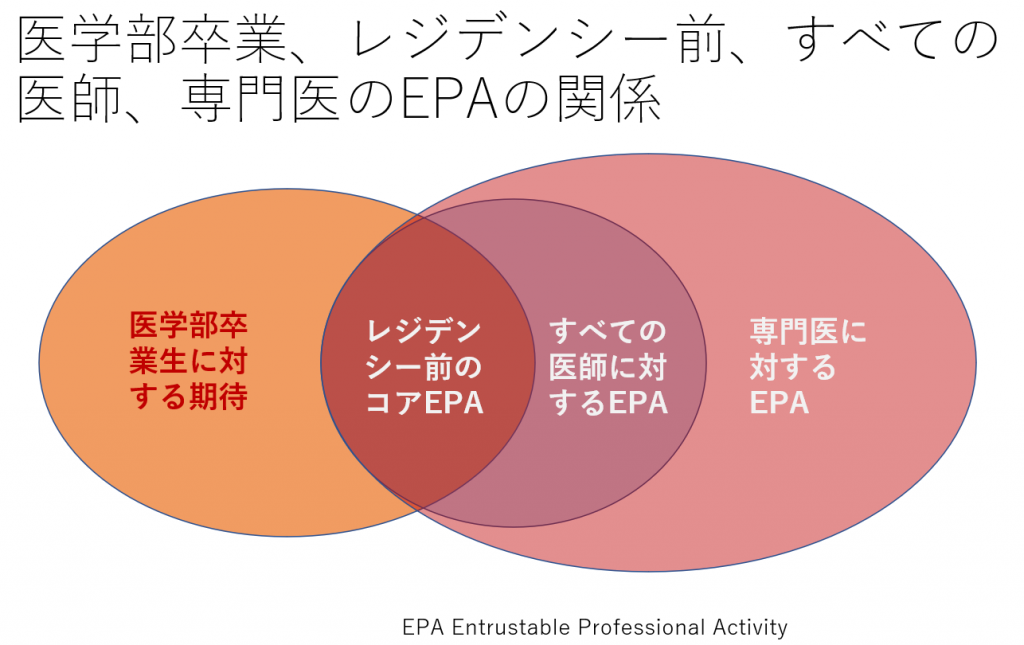

そして、13のEPAに対するツールキットが提供されています。
Core Entrustable Professional Activities for Entering Residency: Toolkits for the 13 Core EPAs.
Contents
EPA 1 Toolkit: Gather a History and Perform a Physical Examination
EPA 2 Toolkit: Prioritize a Differential Diagnosis Following a Clinical Encounter
EPA 3 Toolkit: Recommend and Interpret Common Diagnostic and Screening Tests
EPA 4 Toolkit: Enter and Discuss Orders and Prescriptions
EPA 5 Toolkit: Document a Clinical Encounter in the Patient Record
EPA 6 Toolkit: Provide an Oral Presentation of a Clinical Encounter
EPA 7 Toolkit: Form Clinical Questions and Retrieve Evidence to Advance Patient Care
EPA 8 Toolkit: Give or Receive a Patient Handover to Transition Care Responsibility
EPA 9 Toolkit: Collaborate as a Member of an Interprofessional Team
EPA 10 Toolkit: Recognize a Patient Requiring Urgent or Emergent Care and Initiate Evaluation and Management
EPA 11 Toolkit: Obtain Informed Consent for Tests and/or Procedures
EPA 12 Toolkit: Perform General Procedures of a Physician
EPA 13 Toolkit: Identify System Failures and Contribute to a Culture of Safety and Improvement
13のEPAを翻訳すると以下の通りです。
EPA 1 : 病歴を聴取しと身体診察を実施する
EPA 2 : 臨床的な遭遇の後、鑑別診断の優先順位を決める
EPA 3 : 一般的な診断検査およびスクリーニング検査を推奨し解釈する
EPA 4 : オーダーと処方箋を入力し、議論する
EPA 5 : 患者記録に臨床的な遭遇を記録する
EPA 6 : 臨床的な遭遇について口頭で説明する
EPA 7 : 患者ケアを促進するためのクリニカルクエスチョンを作成し、エビデンスを収集する
EPA 8 : ケア責任を移行するための患者引き渡しを実施するまたは受領する
EPA 9 : 専門家間チームのメンバーとして協力する
EPA 10 : 緊急または救急ケアが必要な患者を認識し、評価と管理を開始する
EPA 11 : 検査や処置のためのインフォームドコンセントを取得する
EPA 12 : 医師としての一般的な手順を実行する
EPA 13 : システムの不具合を特定し、安全と改善の文化に貢献する
利用ガイドとして次の様に述べられています。このツールキットは、「レジデント開始時の中核的な委託可能な専門的活動(EPA)」の実施に関心のある医学部向けのものです。AAMC Core EPA Pilot Groupによって書かれたこのツールキットは、EPA Developer’s Guide(AAMC 2014)に概説されているEPAのフレームワークを拡張したものです。パイロットグループは、学生が医学部のカリキュラムに参加し、臨床技能を統合することに熟達するにつれて、医学教育者が遭遇する可能性のある学生の行動の段階的なシーケンスを特定しました。これらの一連の行動は、EPAを理解するための枠組みを提供するために、13のEPAそれぞれについて1ページの図式で明確にされています。
EPAがどのようなものかは、Toolkits for the 13 Core Entrustable Professional Activities for Entering Residency. Washington, DC: Association of American Medical Colleges; 2017を読まないとなかなか理解できないかもしれません。上記のリンクからFull Toolkit (PDF)を開いてみてください。13のツールキットに関してひとつのファイルとしまとめられています。
Englander Rらの論文から重要用語概念の定義について紹介しておきます。
-コンピテンシーフレームワーク: “相互に関連し、目的を持った一連のコンピテンシーを組織的、構造的に表現したもの”
-コンピテンスのドメイン(領域): 広範な区別できるコンピテンシーの領域で、集合体として専門職の一般的な記述的な枠組みを構成するもの。(著者の定義)
-コンピテンシーリスト:コンピテンシーフレームワーク内の具体的なコンピテンシーを定義したもの。(著者の定義)
-コンピテンス: “ある文脈におけるパフォーマンスの複数の領域または側面にわたる一連の能力 abilities(知識、技能、態度、または KSA)」。コンピテンスに関する記述には、関連する能力、文脈、および訓練の段階を定義するための説明的な修飾子が必要である。コンピテンスは多次元的かつ動的なものである。それは、時間、経験、設定によって変化する” KSA: Knowledge, Skills, Attitudes
-コンピテンシー:”知識、技能、価値観、態度などの複数の要素を統合した、医療専門家の観察可能な能力。コンピテンシーは観察可能であるため、その習得を確認するために測定・評価することができる。”
Englander R, Cameron T, Ballard AJ, Dodge J, Bull J, Aschenbrener CA: Toward a common taxonomy of competency domains for the health professions and competencies for physicians. Acad Med 2013;88:1088-94. doi: 10.1097/ACM.0b013e31829a3b2b PMID: 23807109
Core Entrustable Professional Activities for Entering Residency: Curriculum Developers’ Guideには、13のEPAについて、それぞれ、活動の記述、最も関連のあるコンピテンシーのドメイン、それぞれのドメイン内で委託可能な決断にとって重大な(Critical)コンピテンシー、およびそれぞれの重大なコンピテンシーについて、委託可能前の行動(Behaviors)、委託可能な行動について記述が表にまとめられています。表に続いて、委託可能前の学習者の場合の期待される行動と例、委託可能な学習者の期待される行動と例に対する記述があります。
例えば、EBMに関連のあるEPAである”EPA 7 : 患者ケアを促進するためのクリニカルクエスチョンを作成し、エビデンスを収集する”は、それぞれのドメイン内で委託可能な決断にとって重大なコンピテンシーとして、KP 3, KP 4, PBLI 1, PBLI 3, PBLI 6, PBLI 7, PBLI 9, ICS 2が挙げられています。
例えば、KP 3は、”臨床科学の確立された原理と新しい原理を、診断と治療の意思決定、臨床上の問題解決、およびエビデンスに基づくヘルスケアのその他の側面に適用する”というコンピテンシーです。
Appendix CがReference List of General Physician Competencies by Domainで最初に紹介した、PC, KP, PBLI, ICS, P, SBP, and IPC, PPDのコンピテンシーがリストアップされていますので、その他のコンピテンシーについても確認することができます。
日本の場合は、平成28年度改訂版 医学教育モデル・コア・カリキュラム 133ページに 医師として求められる基本的な資質・能力の項に、9つの項目が挙げられており、134ページからは、臨床実習の到達目標として9つの項目が挙げられています。さらに、141ページ 臨床実習で学生を信頼し任せられる役割(EPA: Entrustable Professional Activities)として、13項目について5段階評価のための表が掲載されています。アメリカの場合と比べると、ほぼ同じ項目が含まれていますが、相違もあります。
ACGME (Accreditation Council for Graduate Medical Education) 米国卒後医学教育認定評議会は卒後教育におけるマイルストーンMilestonesを設定しています。Milestone Resourcesでさまざまな資料が公開されています。
ACGME Milestones Guidebook for Residents and Fellowsには、Competency-Based Medical Education (CBME)についての解説があります。その部分を翻訳すると以下の通りです。
”ポイント
●CBME は、主要な能力領域(すなわちコンピテンシー)を使用して、カリキュラムの設計とプログラムの評価を行います。
●CBMEは、資格取得に必要な特定の時間に基づくのではなく、医療行為に必要な標準的な能力のレベルに到達することに重点を置いています。
●内容、進行、および評価は、個々の学習者が発揮する能力に基づいて行われます。
●CBME は、研修医、フェロー、教員、プログラム、認定機関、および一般市民が共有するモデルを作成します。
●CBMEは、研修医やフェローが改善のために自ら行動計画を立てられるよう、より良いフィードバック、コーチング、振り返りを可能にします。
CBMEとは?
CBMEは、コアコンピテンシーやマイルストーンの実施を含め、研修医やフェローの教育に利用されてきました。文献によると、CBMEは「コンピテンシーという組織的枠組みを用いて、医学教育プログラムの設計、実施、評価を行うアウトカムベースのアプローチ」と定義されています(Frank et al.2010)。コンピテンシーとは、誰かが仕事をするために必要な主要な能力の集合を表すものである。例えば、将来医師となる人は皆、患者ケアを行うための基本的な知識と能力を備えていなければなりません。これらの重要な能力がなければ、仕事を遂行することはできません。
CBMEは、卒業するすべての学習者が、実践で患者をケアするための重要な分野における基本的な能力を獲得することを目的としています。研修医、フェロー、その他の医師は、これらの能力を獲得したことを示すことができるはずです。注目すべきは、これは、教育やトレーニングが純粋に何年修了したか(例えば、内科の場合は3年)に基づくモデルとは異なるということです。”
Frank JR, Snell LS, Cate OT, Holmboe ES, Carraccio C, Swing SR, Harris P, Glasgow NJ, Campbell C, Dath D, Harden RM, Iobst W, Long DM, Mungroo R, Richardson DL, Sherbino J, Silver I, Taber S, Talbot M, Harris KA: Competency-based medical education: theory to practice. Med Teach 2010;32:638-45. doi: 10.3109/0142159X.2010.501190 PMID: 20662574