OECD Education 2030 projectは、2015年から始まった、2030年において子ども達に求められるコンピテンシーを検討するとともに、そうしたコンピテンシーの育成につながるカリキュラムや教授法、学習評価などについて検討していくプロジェクトです。その最終報告書のひとつの仮訳「OECD ラーニング・コンパス(学びの羅針盤)2030」が文部科学省により公開されています。OECD Future of Education and Skill 2030はこちらです。ここではさまざまな資料が提供されています。
OECD (Organisation for Economic Co-operation and Development)は経済協力開発機構です。医学教育に直接関係ないのですが、このプロジェクトの中間報告は教育学の進歩が取り入れられ、未来に向けた教育の在り方が述べられており、素晴らしい内容です。
中間報告のFigure 1を書き直したものが図1です。
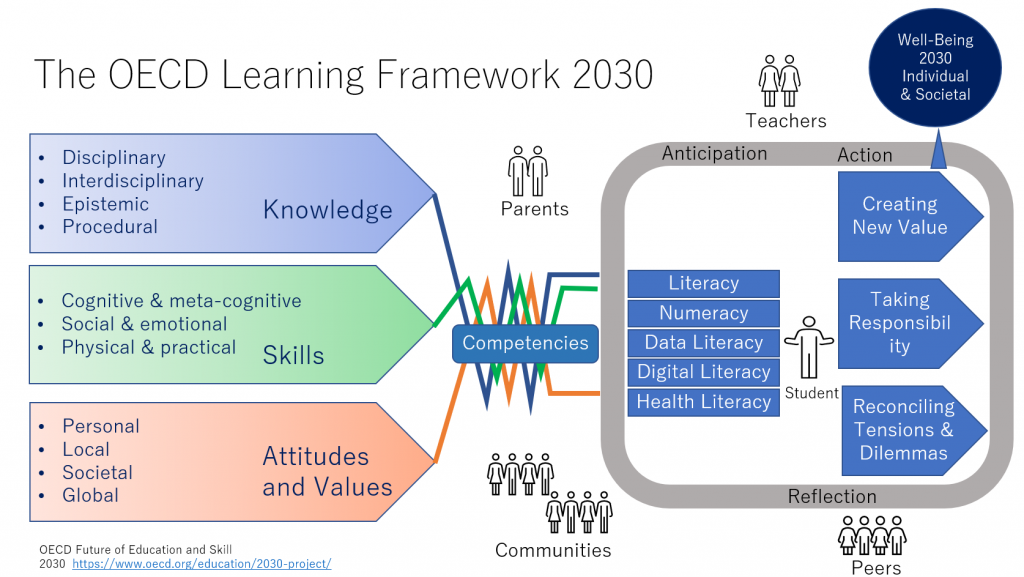
左側の知識、スキル(技能)、態度と価値観が絡み合って、中央のコンピテンシーを構成することが表されています。このような教育を受けた人は、新しい価値を創造し、ちゃんと責任をとり、緊張やジレンマを融和させ、個人としても社会としてもWell-beingな状態になる。WHOのいうWell-beingウェルビーイングと同じですね。WHOのWell-beingについては、こちら、Health Promotion Glossary Terms 2021はこちら(PDF)を参照してください。
コンピテンシーCompetencyとは:
「コンピテンシーという概念は、単なる知識やスキルの習得にとどまらず、複雑な要求に応えるための知識、スキル、態度、価値観を総動員することを意味する。将来に準備ができている学生には、幅広い知識と専門的な知識の両方が必要とされる。」
知識は、•分野別の知識 、多くの分野についての(学際的)知識、•認識論的知識、
例えば、数学者、歴史家、科学者のように考えるにはどうしたらよいかを知ること、
•手続き的知識に分類されています。
スキルも、・認知-メタ認知スキル(批判的思考、創造的思考、学習、自己制御など)、・社会・感情スキル(共感、自己効力感、コラボレーションなど)、・実践・身体スキル(新しい情報通信技術機器の使用など)に分類されています。
態度・価値観は、・個人、・地域、・社会、・世界に分類されています。
そして、•学生は、未知の状況や進化する状況において、自分の知識を応用する必要があり、そのためには、認知・メタ認知スキル(批判的思考、創造的思考、学習、自己制御など)、社会・感情スキル(共感、自己効力感、コラボレーションなど)、実践・身体スキル(新しい情報通信技術機器の使用など)など、幅広いスキルが必要となる。
知識の詰め込みではなく知識の応用ができないといけない、正解のない問題に対処できないといけない、等々言われていますが、そのためには、応用可能な形で、正しい知識を幅広く身に着けている必要があり、いままでの詰め込み以上の知識が要求されると思います。そして、・スキル・態度-価値観についても同様です。このような教育を受けてこなかった、今の大人たちは、自分たちには欠けたものがあることを認識したほうがいいかもしれません。
用語:
•Epistemology認識論: How we know?を論ずる学問。知識とは何か?知識はどのように獲得されるか?人々は何を知るか?何を知っているかをどのように知るか?人間の知識は信頼できるか?我々の感覚は信頼していいか?意見、知識、知恵の違いは何か?
•Epistemic knowledge 認識論的知識
•認知能力:知識の習得、情報の操作、推論において必要とされる脳を使った能力。
•メタ認知:メタ認知とは、自分の認知処理を監視し、適応的に制御する能力、または思考について考える能力のこと。自分の記憶を自覚することで、必要な知識が不足している状況を回避することができる機能。
コンピテンシーの概念が理解できていないと、Reusable Learning Object (RLO)のこともよくわからないと思いますし、マルチメディア学習デザインプリンシプルも、Entrustable Professional Activity (EPA)のこともよくわからないかもしれません。

